
AUTEUR DE L’ARTICLE
Docteur vétérinaire Marine ROCHE-CATHOLY – Unité de cardiologie
Résumé des recommandations du consensus ACVIM pour la classification, le diagnostic et le traitement des cardiomyopathies chez le chat
Les cardiomyopathies représentent un groupe hétérogène de maladies myocardiques de phénotype et pronostic très variables.
Le dépistage de ces affections en l’absence de signe clinique ou leur diagnostic lorsque ces signes sont présents, constituent un motif de consultation fréquent en médecine vétérinaire féline, et placent les maladies cardiovasculaires parmi les 10 causes de décès les plus fréquentes dans cette espèce.
En 2020, un panel de neuf experts internationaux de la cardiologie vétérinaire ont publié leurs recommandations quant à la classification, au diagnostic et au traitement des cardiomyopathies chez le chat. Nous vous proposons ici un résumé non exhaustif de cette publication disponible en libre accès.
Définition et classification des cardiomyopathies chez le chat
Chez l’homme, une cardiomyopathie est définie comme une affection du myocarde entraînant une altération de sa structure et de sa fonction, en l’absence de tout autre maladie cardiovasculaire pouvant en être à l’origine ; différentes classifications de ces cardiomyopathies ont été proposées, notamment en fonction de leur cause.
Chez le chat, la cause des cardiomyopathies étant rarement identifiée avec certitude, les experts du consensus ACVIM ont proposé une classification basée sur leurs phénotypes échocardiographiques, même si cette classification comporte des limites, car chez certains chats, le phénotype peut changer au cours du temps. Ces cardiomyopathies de différents phénotypes comprennent les cardiomyopathies d’origine connue (comme celles secondaires à une hyperthyroïdie ou une mutation génétique par exemple) et celles d’origine inconnue. Tant que la cause sous-jacente n’est pas connue, les chats sont décrits comme présentant une cardiomyopathie de tel ou tel phénotype : par exemple, une hypertrophie ventriculaire gauche de cause inconnue sera qualifiée de « cardiomyopathie de phénotype hypertrophique » mais si le chat présente également une hyperthyroïdie, la cardiomyopathie sera alors qualifiée comme « cardiomyopathie de phénotype hypertrophique associée à une hyperthyroïdie ».
Lorsque les caractéristiques d’une cardiomyopathie ne correspondent à aucun des phénotypes listés dans le tableau ci-dessous, plutôt que de qualifier cette cardiomyopathie d’inclassable comme cela était le cas auparavant, le terme de « cardiomyopathie de phénotype non spécifique » doit être employé, et ses caractéristiques morphologiques et fonctionnelles doivent être détaillées.
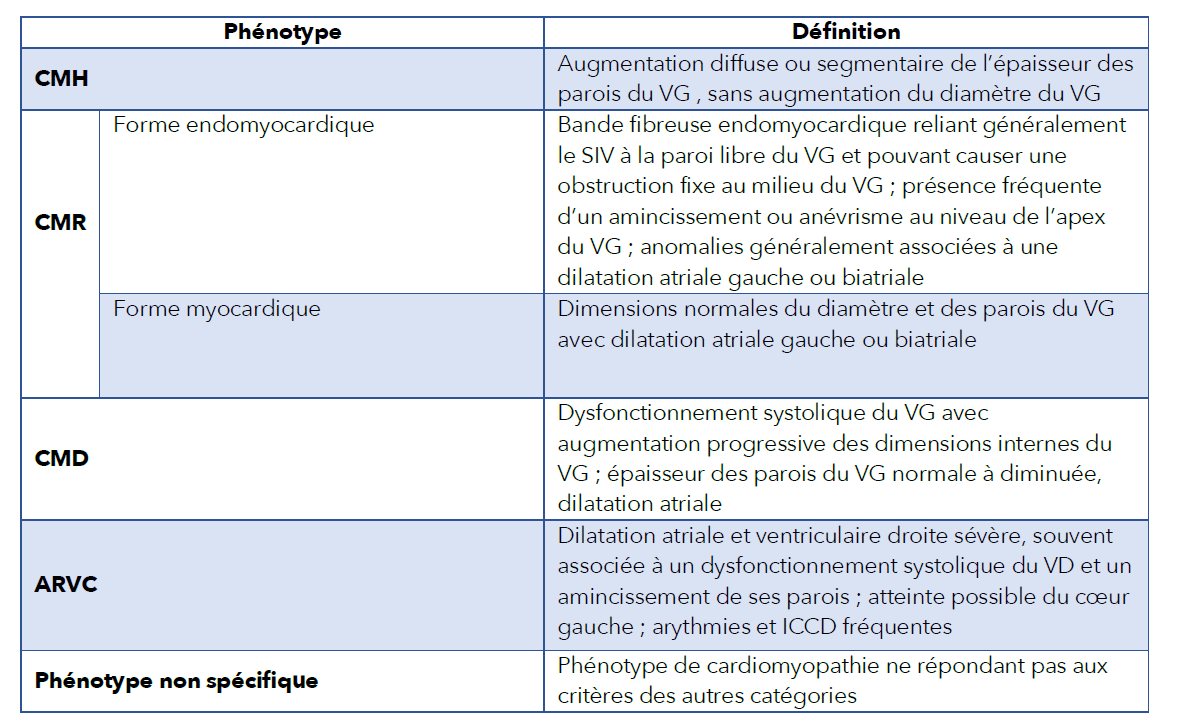
Tableau 1 : définition des phénotypes de cardiomyopathie
Abréviations : CMH = cardiomyopathie hypertrophique, CMR = cardiomyopathie restrictive, CMD = cardiomyopathie dilatée, ARVC = cardiomyopathie ventriculaire droite arythmogène, ICCD = insuffisance cardiaque congestive droite ; VD = ventricule droit ; VG = ventricule gauche, SIV = septum interventriculaire
A l’instar des stades A, B, C, D utilisés dans la maladie dégénérative de la valve mitrale chez le chien, le panel d’experts propose également de classer les cardiomyopathies félines selon les mêmes stades précliniques et cliniques, afin de guider les prises de décisions thérapeutiques, ainsi que pour aider à établir un pronostic.

Figure 1 : stades cliniques des cardiomyopathies félines.
Chez les individus en stade B1 la dilatation atriale gauche est absente ou faible et ces chats présentent un faible risque d’insuffisance cardiaque congestive ou de thromboembolie artérielle. Les individus en stade B2 présentent une dilatation atriale gauche modérée à sévère et un risque plus élevé d’insuffisance cardiaque congestive ou de thromboembolie artérielle. Les facteurs de risque supplémentaires impliquant un classement en stade B2, sont la présence d’un bruit de galop, d’arythmies, une diminution de la fonction systolique atriale gauche, un épaississement majeur des parois ventriculaires gauches, un dysfonctionnement systolique du ventricule gauche, la présence d’un contraste échographique spontané ou d’un thrombus, et des anomalies régionales de déplacement des parois myocardiques (mode Doppler tissulaire).
Abréviations : ICC insuffisance cardiaque congestive ; TEA thromboembolie artérielle
Diagnostic des cardiomyopathies chez le chat
L’échocardiographie (figure 1) est l’examen de choix pour diagnostiquer les cardiomyopathies félines, bien que la différenciation entre les phénotypes reste parfois délicate, même pour des spécialistes.
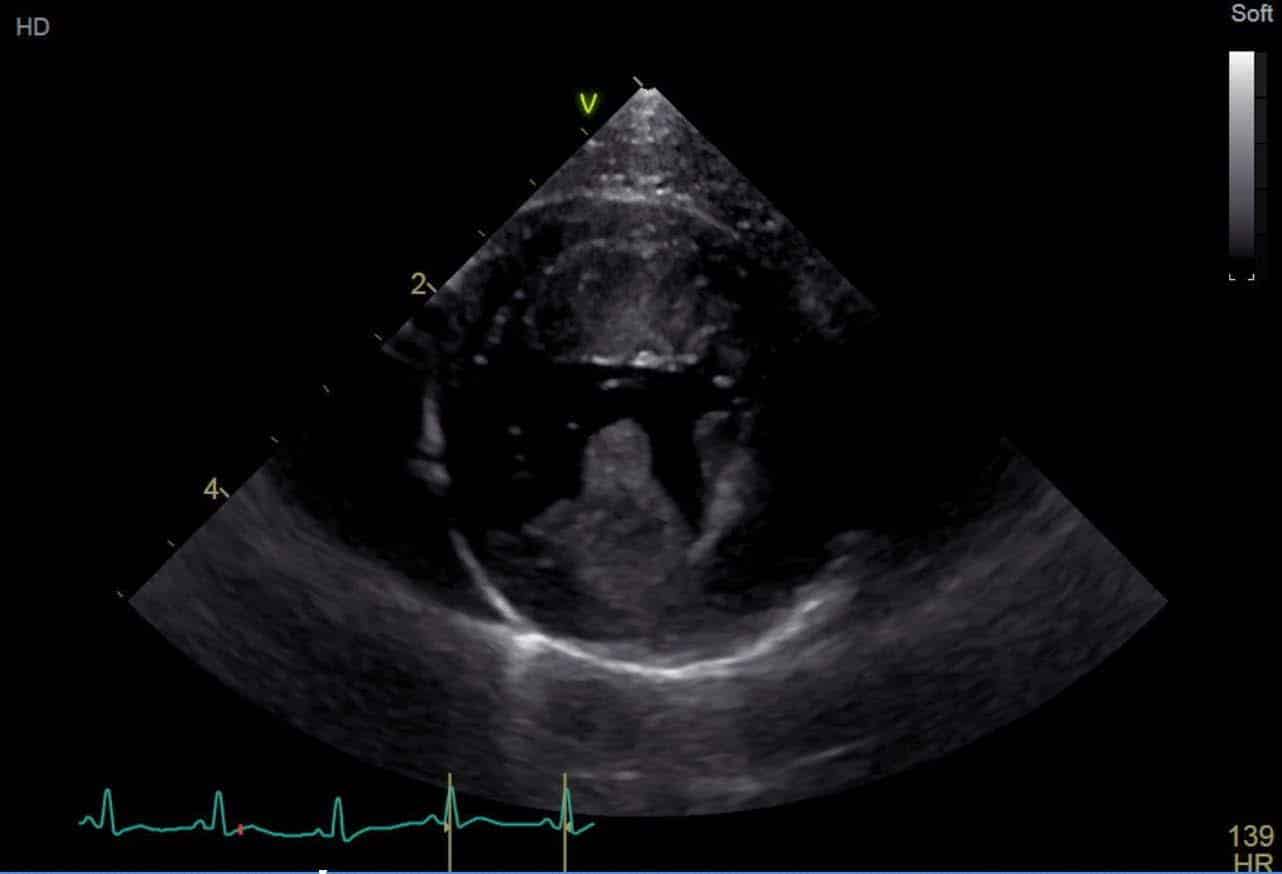
Figure 2 : image échocardiographique (coupe petit axe transventriculaire par abord parasternal droit) mettant en évidence la présence d’une cardiomyopathie de phénotype hypertrophique, avec épaississement symétrique du septum interventriculaire et de la paroi libre ventriculaire gauche, et hypertrophie des muscles papillaires
Les mutations MyBPC3-A31P et MyBPC3R820W à l’origine d’une CMH ont été identifiées chez le Maine Coon et le Ragdoll respectivement, et le test génétique est donc réservé à ces 2 races, en particulier chez les reproducteurs. Néanmoins, certains chats négatifs pour cette mutation peuvent tout de même développer une cardiomyopathie (dont CMH), ce qui illustre l’intérêt des dépistages échocardiographiques même chez les chats appartenant aux races précitées.
Jusqu’à 80% des chats en stade préclinique présentent un souffle cardiaque systolique parasternal audible à l’auscultation, alors qu’un souffle n’est présent que chez 30-45% des chats sains. Un bruit de galop (2,6-19% des chats) ou des arythmies sont également rapportés chez les chats présentant une CMH préclinique. Ces anomalies auscultatoires doivent donc inviter à la réalisation d’un examen cardiologique complet.
Chez les animaux en insuffisance cardiaque congestive, des troubles respiratoires sont observés. Des râles crépitants ou une diminution de l’intensité des bruits cardiaques peuvent être détectés à l’auscultation des champs pulmonaires en cas d’œdème pulmonaire ou d’épanchement pleural respectivement.
La réalisation de clichés radiographiques thoraciques (figure 2) peut laisser suspecter la présence d’une cardiomyopathie en cas de visualisation d’une cardiomégalie sévère ou d’une ectopie atriale gauche. Cependant, la radiographie reste peu sensible pour détecter les remodelages cardiaques discrets à modérés, et ne permet généralement pas de préciser le phénotype de la cardiomyopathie. Contrairement à l’espèce canine, le pattern radiographique associé à l’œdème pulmonaire cardiogénique est très variable chez le chat.
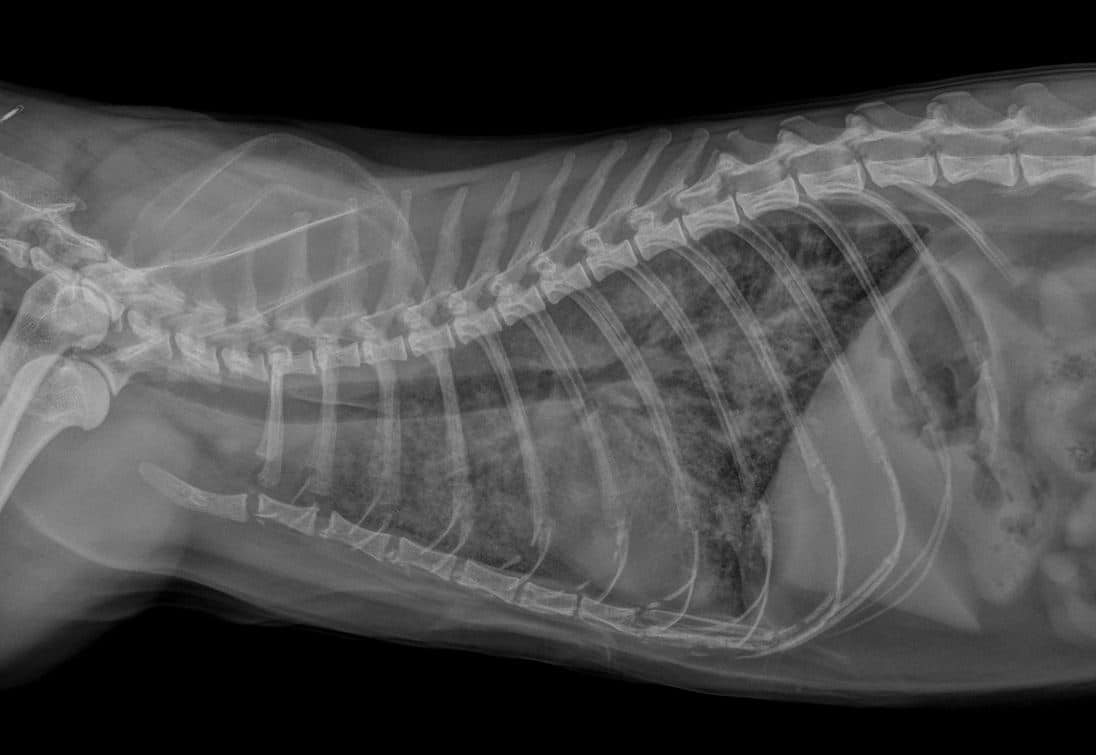
Figure 3 : cliché radiographique thoracique mettant en évidence un œdème pulmonaire cardiogénique sévère, avec opacification des champs pulmonaires chez un chat en détresse respiratoire
Lorsque la radiographie thoracique est indisponible, ou lors de détresse respiratoire majeure, il peut être avisé de réaliser une échographie thoracique d’urgence (Point-Of-Care UltraSound – « POCUS ») pour rechercher des « lignes B » (figure 3), artéfacts échographiques compatibles, bien que non spécifiques, de la présence d’un œdème pulmonaire, ainsi que pour évaluer subjectivement le diamètre de l’atrium gauche et la présence d’un épanchement péricardique (très spécifique d’une insuffisance cardiaque congestive).
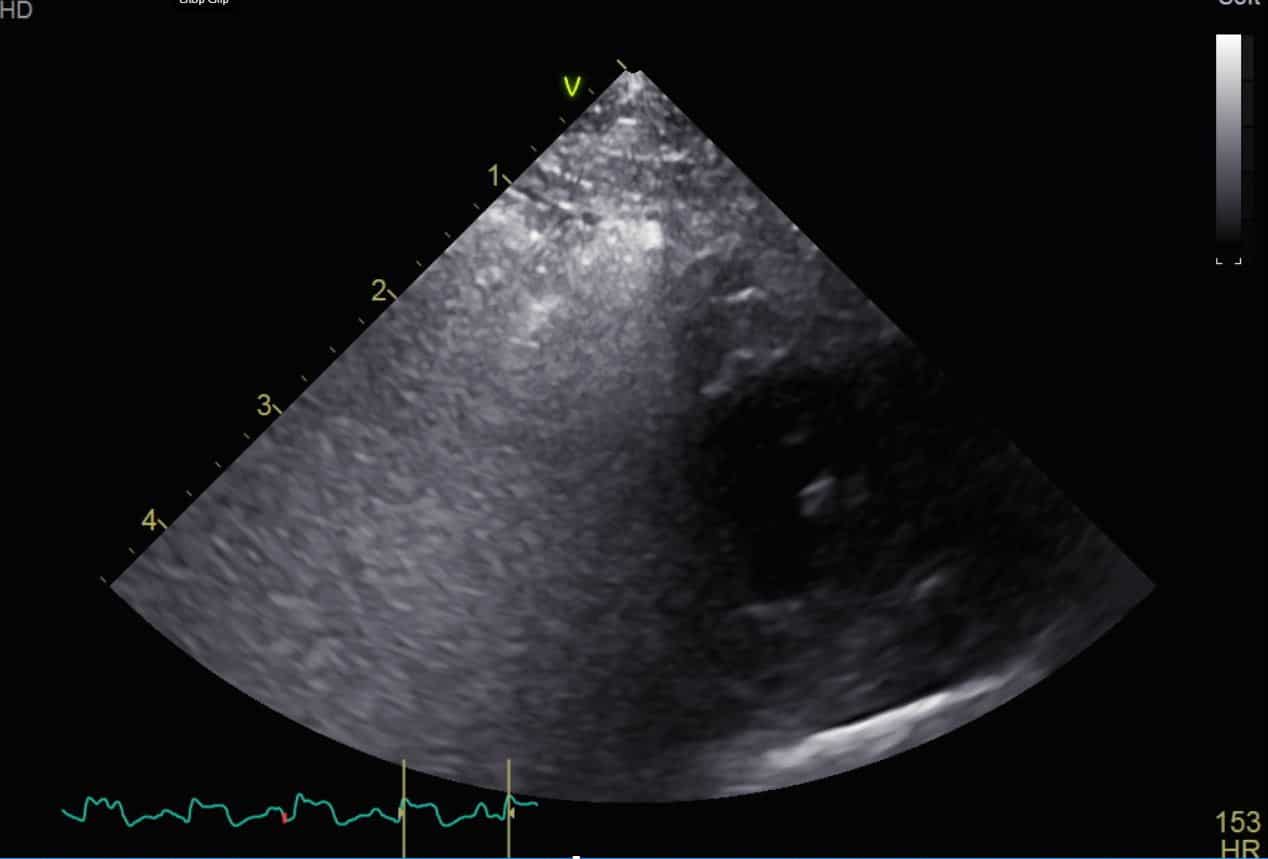
Figure 4 : image échocardiographique mettant en évidence la présence de lignes B coalescentes masquant la silhouette cardiaque et compatibles avec un œdème pulmonaire cardiogénique chez un chat présenté pour détresse respiratoire
Dans ce cas de figure, la réalisation d’un test SNAP NT-proBNP permet également d’orienter le diagnostic entre l’origine cardiaque et extracardiaque de la détresse respiratoire. Au chevet du patient, l’association des résultats de l’examen clinique, de l’échographie d’urgence POCUS et du SNAP NT-proBNP permet d’aider le clinicien dans sa démarche diagnostique dans le cadre des détresses respiratoires.
La réalisation d’un électrocardiogramme (ECG) ne permet pas de diagnostiquer les cardiomyopathies du chat, et n’est recommandée que dans l’optique de caractériser les arythmies associées présentes.
Afin d’investiguer les causes possibles de cardiomyopathie, il est recommandé de réaliser une mesure de pression artérielle ainsi qu’un dosage de la thyroxine (T4) à partir de 6 ans d’âge ; néanmoins lors d’hyperthyroïdie, si l’hypertrophie des parois du ventricule gauche est marquée, une cardiomyopathie associée doit être suspectée. Dans l’hypothèse d’une cardiomyopathie dilatée, le régime alimentaire doit être précisé auprès du propriétaire, et le dosage de la taurine pourra être envisagé en cas de doute.
Traitement des cardiomyopathies chez le chat Stade B1
A ce stade, le risque d’insuffisance cardiaque congestive ou de thromboembolie artérielle est faible, et aucun traitement n’est actuellement recommandé. La présence d’une obstruction dynamique de la chambre de chasse du ventricule gauche (figure 4) n’a pas démontré qu’elle péjorait le pronostic, et la mise en place d’un traitement à l’aténolol n’a montré aucun effet significatif sur le taux de survie chez les chats atteints de CMH en stade préclinique. Néanmoins, certains auteurs emploient de l’aténolol chez les chats présentant une obstruction dynamique sévère de la chambre de chasse du ventricule gauche, de par son intérêt à pouvoir diminuer le degré d’obstruction.
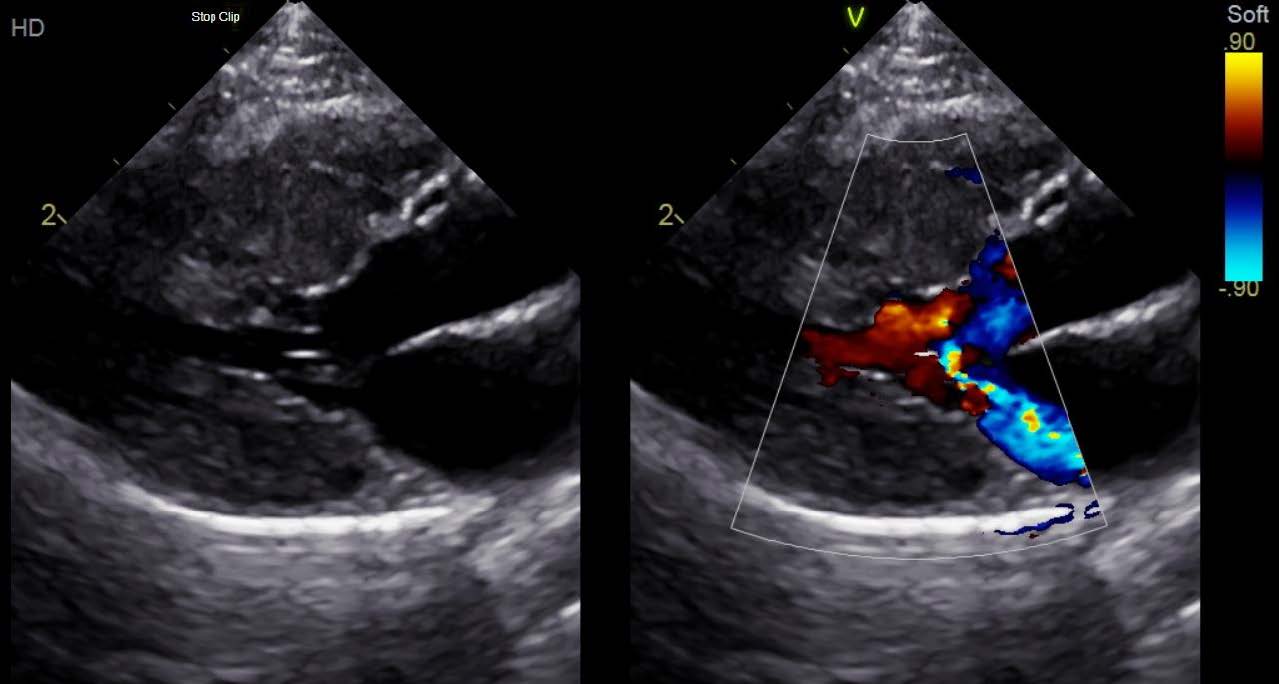
Figure 5 : image échocardiographique 2D (A) et Doppler couleur (B) (coupe 5 cavités par abord parasternal droit) mettant en évidence un mouvement systolique antérieur du feuillet septal mitral (flèche jaune) associé à une obstruction dynamique de la chambre de chasse du ventricule gauche et une insuffisance mitrale excentrée.
Stade B2
Les chats en stade B2 (présentant une dilatation atriale modérée à sévère) sont à risque accru de développer une insuffisance cardiaque congestive ou une thromboembolie artérielle. Il est actuellement recommandé de réaliser une thromboprophylaxie chez ces individus (figure 5), ainsi que chez ceux présentant une diminution de la fonction systolique atriale gauche, et/ou une diminution de la vélocité du flux sanguin dans l’auricule gauche. Une étude prospective randomisée a établi la supériorité en termes d’efficacité du clopidogrel par rapport à l’aspirine. A ce stade, il est également conseillé de procéder à
une surveillance de la fréquence respiratoire pendant le sommeil, par le propriétaire. Des études randomisées n’ont montré aucun effet significatif des inhibiteurs de l’enzyme de conversion de l’angiotensine (IECA – ramipril et bénazépril) ou de la spironolactone en stade préclinique. Il est actuellement recommandé de traiter les chats présentant des arythmies ventriculaires, avec de l’aténolol (6.25 mg/chat q12h PO) ou du sotalol (10-20 mg/chat q12h PO). Le diltiazem, l’aténolol ou le sotalol peuvent être envisagés en cas de fibrillation atriale à réponse ventriculaire rapide.
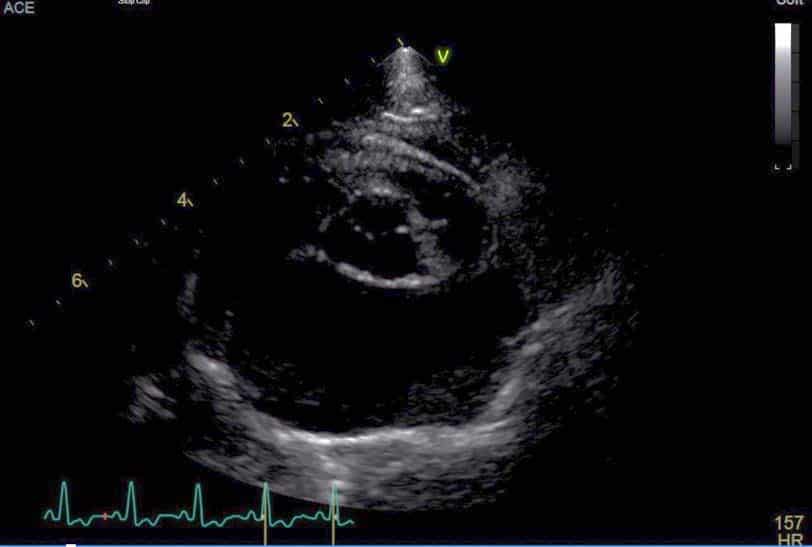
Figure 6 : image échocardiographique (coupe petit axe transaortique par abord parasternal droit) mettant en évidence une dilatation atriale et auriculaire gauche.
Stade C
Insuffisance cardiaque congestive aigüe
Les animaux sont généralement présentés en tachypnée et/ou dyspnée. Le stress secondaire aux manipulations doit être minimisé au maximum, et une oxygénothérapie doit être initiée dès que possible ; une sédation peut également être réalisée (exemple : butorphanol). Le furosémide peut être administré par bolus IV de 1-2 mg/kg et répété, ou administré en perfusion continue (CRI = Constant Rate Infusion). Une thoracocentèse doit être réalisée lorsque la détresse respiratoire résulte d’un épanchement pleural. L’administration de fluides est contre-indiquée chez les chats présentant des signes cliniques d’œdème ou d’épanchement, même si des diurétiques ont été initiés concomitamment.
Sur les chats présentant des signes de bas débit cardiaque (hypotension, hypothermie, bradycardie), l’administration de pimobendane peut être envisagée. Les IECA ne sont pas recommandés lors de la phase aigüe de l’insuffisance cardiaque. Les paramètres rénaux doivent être monitorés afin de s’assurer de la bonne tolérance du traitement diurétique.
Insuffisance cardiaque chronique
Le traitement des stades chroniques repose principalement sur l’emploi de furosémide, généralement administré à une dose comprise entre 0,5 et 2 mg/kg q8-12h PO, en ciblant la dose minimale efficace permettant de maintenir la fréquence respiratoire en dessous de
30 mouvements/minute. Une étude randomisée n’a pas montré d’effet significatif du bénazépril sur l’augmentation du délai conduisant à un échec thérapeutique (mortalité, euthanasie, ou insuffisance cardiaque congestive réfractaire) sur des chats en insuffisance
cardiaque congestive, bien que certains cardiologues l’emploient tout de même en stade C chronique. Une thromboprophylaxie avec du clopidogrel (18,75 mg/chat PO q24h) est conseillée. Le pimobendane peut également être envisagé (0,625-1,25 mg/chat q12h PO), en l’absence d’obstruction significative de la chambre de chasse du ventricule gauche.
Stade D
Il peut être envisagé de changer de diurétique de l’anse (torasémide à la place de furosémide), chez les chats présentant des signes d’insuffisance cardiaque réfractaire à des doses de furosémide dépassant 6 mg/lg/jour PO, en débutant par 0,1-0,2 mg/kg PO q24h. Certains cardiologues emploient également de la spironolactone (1-2 mg/kg PO q12-24h). Chez les chats présentant un dysfonctionnement systolique, l’ajout de pimobendane est recommandé.
Traitement des thromboembolies artérielles
La priorité dans la prise en charge des thromboembolies artérielles est l’analgésie, et l’emploi de fentanyl ou de méthadone est recommandé. Un traitement anticoagulant est indiqué, avec l’emploi d’héparine de bas poids moléculaire, d’héparine fractionnée, ou d’un inhibiteur du facteur Xa. A l’heure actuelle, les traitements thrombolytiques (exemple : tPA = activateur tissulaire du plasminogène) ne sont pas recommandées chez le chat.
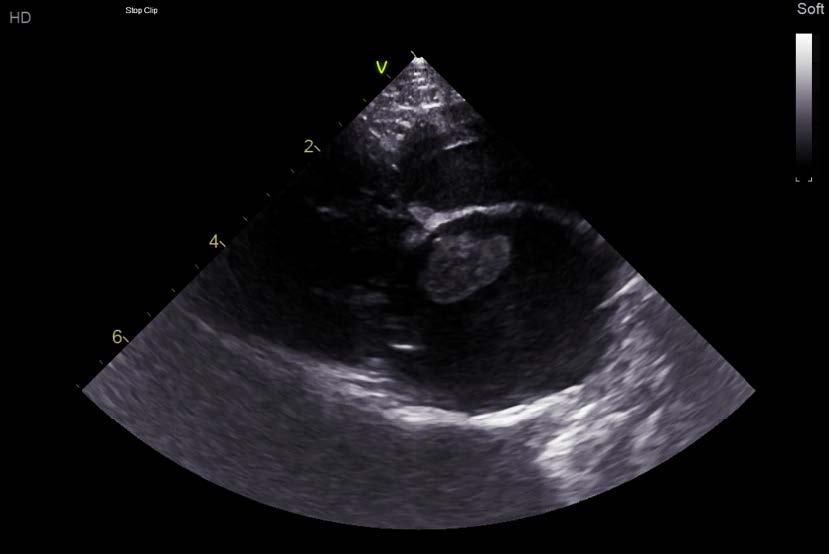
Figure 7 : images échocardiographique (coupe 4 cavités par abord parasternal droit) mettant en évidence une dilatation atriale gauche ainsi que la présence d’un large thrombus (flèche) au sein de l’atrium gauche.
Conclusion
Les cardiomyopathies félines sont un groupe hétérogène d’affections myocardiques dont l’origine est rarement identifiée, et pour lesquelles le pronostic vital peut être rapidement engagé. Il est essentiel de réaliser un examen cardiologique incluant un examen échocardiographique complet dans la mesure du possible, afin de préciser le phénotype, mais surtout de classer le stade de la maladie, et de ce fait d’identifier les individus à risque de complications, pour pouvoir mettre en place un traitement et un programme de surveillance adéquats.



